03 解讀密碼:DNA問世
克里克極力主張,DNA必定是稍後的發展,DNA的「崛起」,原因可能在於RNA分子相對較不穩定,比DNA分子容易發生降解和突變。如果要有一個能夠長期而且穩定地儲存遺傳數據的分子,DNA顯然比RNA適合得多。
布雷納從小在南非約翰內斯堡外的小鎮長大,住家就是父親那間補鞋店後面的兩個房間。雖然來自立陶宛的移民老布雷納並不識字,但他早熟的兒子在4歲時就愛上讀書,後來在一本名為《生命科學》(The Science of Life)的教科書影響下,這股熱情轉向生物學。布雷納日後承認他從公共圖書館偷走了這本書,但盜竊和貧窮都不能阻礙布雷納發展。他14歲便進入威特沃特斯蘭德大學(University of Witwatersrand),專攻醫學課程。他在我們發現雙螺旋一個月後來到劍橋時,正在牛津大學攻讀博士學位。他回想起自己看到我們那個模型時的反應:「當時我一看到它便知道這就是了。在那一瞬間,你知道這是非常基礎性的。」
加羅德進一步觀察到,儘管黑尿症病患佔總人口的比例很低,但顯然比較常見於近親通婚的子女身上。到了1902年,他終於可以用重新「出土」的孟德爾定律來解釋這種現象。罕見隱性基因的遺傳模式如下:如果一對堂兄妹各自從同一位祖父母遺傳到黑尿症的一份基因,則他們結婚後生下的子女將有1/4的幾率會得到純合型(homozygous)基因(即同時擁有兩個隱性基因),並在未來罹患黑尿症。加羅德在結合生化與遺傳分析后,推論黑尿症是一種「先天的新陳代謝錯誤」。雖然當時沒有人真的了解他的研究,加羅德仍是第一位在基因與其生理影響之間找出因果關係的人。基因以某種方式控制新陳代謝的過程,而基因出錯(即突變)可能造成代謝路徑發生缺陷。
現在我們可以把整個故事串連起來,以血紅素蛋白質為例,看看特定的蛋白質是如何製造的。紅血球專門運輸氧氣:它們利用血紅素,把氧氣從肺輸送至需要氧的組織。紅血球是在骨髓中由幹細胞(stem cell)製造出來的,速率驚人,大約每秒可以造出250萬個紅血球。
在進行一連串的實驗后,他們發現在缺乏乳糖的狀況下,有一種叫做抑制子(repressor)的分子,會阻止β-半乳糖苷酶基因的轉錄。但是有乳糖存在時,乳糖會跟這種抑制子結合,使其無法阻止轉錄,因此乳糖的存在使基因得以轉錄。事實上,雅各布與莫諾發現乳糖的新陳代謝也同時受到控制,這不僅是某個基因在特定時間會被開啟或關閉而已,其他基因也參与了消化乳糖的過程,而這個抑制子系統負責調節所有的基因。雖然就基因開關作用的研究而言,大腸桿菌的系統相對簡單,但後續對更複雜的生物體(包括人類)所作的研究顯示,相同的基本原則也同樣適用。

伽莫夫在他的實驗室里
伽莫夫在1934年離開蘇聯來到美國。在1948年的一篇論文中,他解釋宇宙中有大量不同的化學元素,跟在大爆炸(Big Bang)早期階段發生的熱核過程有關。這個研究是由伽莫夫和他指導的研究生阿爾法(Ralph Alpher)所作的,所以署名應該是「阿爾法與伽莫夫」,但是伽莫夫卻決定將他朋友貝特(Hans Bethe)的名字加上去,貝特無疑是位極為出色的物理學家,但是對這項研究絲毫沒有貢獻。生性|愛開玩笑的伽莫夫對於這篇論文能署名為「Alpher, Bethe, and Gamow」(讀音極似希臘字母α、β和γ),又剛好在4月1日愚人節發表,感到非常高興。至今,宇宙學家仍將這篇論文稱為αβγ(Alpha-Beta-Gamma)論文。
1960年,在發現第三種RNA,也就是信使RNA (messenger RNA,mRNA)之後,這些矛盾終於獲得解決。信使RNA證實為蛋白質合成的模板。我在哈佛實驗室,以及梅索森、雅各布(Francois Jacob)和布雷納在加州理工學院及劍橋所做的實驗,都顯示核糖體是個分子工廠。信使RNA從兩個核糖體次單位之間通過,就像送入老式計算機的卡片。各自帶著氨基酸的轉移RNA附著到核糖體內的信使RNA上,讓氨基酸在以化學鍵形成多肽鏈前,先排好順序。
現在,再轉回到過去。1966年在冷泉港舉辦的遺傳密碼會議中,瀰漫著一股大功告成的氣氛。密碼已然破解,我們也大致知道DNA如何通過它所指定的蛋白質來控制生命的程序。有些老手認為應該開始研究基因以外的事物。克里克決定跨入神經生物學,他向來不畏艱難,而且對人類大腦的運作特別感興趣。布雷納轉而研究發育生物學,選擇鑽研簡單的線蟲(Nematode worm),因為他相信科學家可以藉由研究這種簡單的生物,揭露基因與發育之間的關聯。今日在我們這一行,線蟲的確成為生物體如何形成的重要信息來源(我們叫它「蟲子」,不必提全名,大家都知道指的是線蟲)。2002年,諾貝爾獎委員會把生理醫學獎頒給布雷納和另兩位長期研究線蟲的科學家——劍橋大學的薩爾斯頓(John Sulston)與麻省理工學院的賀維茲(Bob Hervitz),肯定了線蟲的功用。
不過,蛋白質並非僅是線狀的氨基酸鏈。一旦製造出氨基酸鏈后,蛋白質會摺疊成複雜的構造,有時是自行摺疊,有時則藉助「輔助」分子。蛋白質必須形成這種結構后才會有活躍的生物作用。以血紅素為例,它必須由四條鏈組成后才能發揮作用。其中兩條鏈為同類型,另外兩條是稍有不同的類型。在每條捲曲的鏈的中心,都載有傳輸氧氣的重要關鍵,即鐵原子。如今我們可以使用現代的分子生物學技術,重新審視早期遺傳學的經典研究。對孟德爾而言,造成豌豆有皺皮與光滑之分的機制極為神秘,他只知道這些性狀的遺傳法則——也就是他研究出來的「孟德爾定律」。不過,現在我們已經了解到造成皺皮與光滑這種差異的分子細節。
當時對於RNA在生命的生化謎團中所扮演的角色還不是很清楚。在有些病毒中,例如煙草花葉病毒,RNA所扮演的角色跟其他物種的DNA類似,能為該生物體特有的蛋白質編碼。而在細胞中,RNA必定有參与蛋白質的合成,因為製造眾多蛋白質的細胞通常都富含RNA。即使在我們發現雙螺旋之前,我就認為染色體DNA的遺傳信息,有可能用於製造由互補序列構成的RNA鏈。然後這些RNA鏈可以作為模板,用於指定氨基酸在各自蛋白質中的順序。若是如此,RNA就是DNA與蛋白質之間的中間物。後來克里克將這種DNA→RNA→蛋白質的信息流向稱為「中心法則」(central dogma)。1959年,RNA聚合酶(polymerase)的發現很快成為這種觀點的佐證。幾乎在所有的細胞中,聚合肽都能催化由雙股DNA模板製造單股RNA鏈的過程。
第一個線索出現於19世紀和20世紀交替之際,就在世人重新發現孟德爾的研究之後。加羅德(Archibald Garrod)是一位英國醫師,由於在醫學院的學習進展緩慢,又欠缺對待病人的良好態度,因此無法在倫敦的聖巴多羅買醫院(St. Bartholomew's Hospital)九-九-藏-書行醫,只能朝研究方向發展。他對一類罕見的疾病特別感興趣,這類疾病共同的顯著癥狀是尿液的顏色很奇怪。其中有一種病症叫黑尿症(alkaptonuria),由於這種病的患者所排出的尿液在接觸到空氣後會變成黑色,因此得名,俗稱「黑尿布症候群」(black diaper syndrome)。儘管黑尿看起來挺嚇人,但黑尿症通常並不會致命,然而隨著黑尿的色素在關節與脊柱逐漸累積后,年老時會出現類似關節炎的癥狀。當時醫學界認為這些病患的尿液是因為腸道細菌所製造的物質而變黑的,但是加羅德卻認為,腸道內沒有細菌的新生兒也會出現黑尿,就表示這種物質是由人體本身所製造的。他推論問題在於人體化學機制的缺陷,以他的說法是「新陳代謝出了錯」,也就是說,這可能是某條生化路徑出現嚴重差錯的結果。
伽莫夫1954年提出的理論中有一項假設具有可以測試的優點,因為它牽涉到重疊的DNA三聯體。伽莫夫推測,事實上許多對氨基酸在蛋白質中永遠不可能相鄰排列。因此他熱切地等待更多的蛋白質序列出爐。令他失望的是,愈來愈多氨基酸被發現時是彼此相鄰的,他的假設愈來愈站不住腳。1956年,負責研究纈氨酸(valine, VAL)的布雷納(Sidney Brenner)在分析當時已經發現的所有氨基酸序列之後,終於給了伽莫夫所設想的編碼方式致命性的一擊。
1990年,英國科學家發現皺皮豌豆缺乏一種與處理澱粉有關的酶,澱粉是儲存在豌豆中的碳水化合物。皺皮豌豆所以會形成,是因為處理澱粉的酶發生基因突變(有不相關的DNA插入基因中間)而不起作用。由於突變的結果,豌豆含有的澱粉較少、糖較多,因此在成熟過程中流失的水分較多。然而在水分流失且豆子體積隨之減小時,豌豆外面的種皮沒有跟著縮小,結果形成獨特的皺皮:因為內含物太少,種皮撐不起來。
發現RNA在細胞內具有重要角色后,一個令人好奇的(也是長久以來未獲得解答的)問題隨之浮現:DNA的信息為什麼要通過RNA這個中介,才能轉譯成多肽序列?在解開遺傳密碼后不久,克里克針對這個矛盾的問題提出一個解答:RNA比DNA早出現。他設想當生命是以RNA為基礎時,RNA是第一個遺傳分子,亦即在我們今日熟悉的「DNA世界」出現前,在數十億年前,地球原本是一個「RNA世界」。克里克猜測,RNA不同的化學性質(它的骨幹是核糖,DNA則是脫氧核糖)可能賦予它酶的性質,讓它能催化本身的自我複製。
克里克所提出的在DNA世界之前有一個RNA世界的想法,原本幾乎沒人注意,一直到1983年,事情才改觀。那時科羅拉多大學的切赫(Tom Cech)和耶魯大學的奧特曼(Sidney Altman)分別證實,RNA分子的確具有催化性質,這項發現讓他們贏得1989年的諾貝爾化學獎。10年後,又出現了一個更確鑿的證據,證明在DNA之前的確是RNA世界。核糖體是蛋白質的合成地點,而已知跟核糖體有關的蛋白質有60種,但加州大學聖塔克魯斯分校的諾勒(Harry Noller)卻證明,在蛋白質內將氨基酸連結在一起的肽鍵(peptide bond),並不是在這60種蛋白質中的任意一個催化之下形成的,相反地,肽鍵的形成是由RNA所催化。諾勒去除核糖體所有的蛋白質,發現它仍能形成肽鍵,因而獲得這個結論。其後,諾勒和其他人在對核糖體的立體結構進行精密的分析后,找到了原因:蛋白質散布在核糖體表面各處,遠離核糖體中心的作用地點。
早在艾弗里的實驗讓世人注意到DNA為「轉化因子」之前,遺傳學家就己經試圖了解遺傳物質——不論它究竟為何——如何能影響特定生物體的特徵。換句話說,孟德爾的「因子」如何影響豆子的外形,使它們變皺或光滑?
在發現雙螺旋后的頭20年,分子生物學已經有了長足的進展。我們了解生命基本的運作機器,甚至得以一窺基因的調控方式。但是在當時,我們所做的仍然只是觀察;我們是分子博物學家,細胞就像一座雨林,而我們所能做的就是描述裏面有什麼。但是我們已經觀察夠了,現在到了該採取積極態度的時候:干預,也就是操控生物的渴望召喚著我們。重組DNA技術的出現,以及隨之而來的「調整」DNA分子的能力,將使這一切有可能成真。
尼倫伯格在美國國家衛生研究院(National Institute of Health, NIH)服務,在聽到關於信使RNA的發現后,他開始思索,如果要在無細胞系統中合成蛋白質,在試管內合成的RNA和自然產生的信使RNA,不知其效能是否相同。為了找出結果,他按照6年前法國生化學家格倫伯格-馬納戈(Marianne Grunberg-Manago)在紐約大學發展出的程序來製造RNA。格倫伯格-馬納戈發現一種能製造AAAAAA或GGGGGG等氨基酸鏈的RNA酶。此外,由於RNA與DNA之間一個重要的化學差異在於RNA有尿嘧啶(U),而沒有DNA的胸腺嘧啶(T),因此這種酶也會製造UUUUUU,以生化術語來說,就是聚尿嘧啶(poly-U)。1961年5月22日,尼倫伯格和德國同事馬特伊(Heinrich Matthaei)將聚尿嘧啶加入無細胞系統,結果非常驚人:核糖體開始產生一種簡單的蛋白質,而且全是由同一種氨基酸「苯丙氨酸」(phenylalanine)所組成。他們發現聚尿嘧啶是為苯丙氨酸編碼的,因此,指定苯丙氨酸的三字母遺傳密碼中,必定有一個是UUU。
雅各布在結束面談后,立刻直接跑到書店找字典,查他剛才答應的研究主題究竟是什麼。
但是RNA卻可以提供答案,因為它的功能與DNA相當,能夠儲存與複製遺傳信息,又與蛋白質相當,能夠催化關鍵的化學反應。事實上,在RNA世界,「先有雞,還是先有蛋」的問題根本不存在,因為RNA既是「雞」,也是「蛋」。
諾勒正在研究核糖體。他的實驗可以證明,在生命起源時存在著—個RNA世界。
我回了一聲「喔!」然後竭盡所能地讚美,心裏卻想著:「原噬菌體究竟是什麼玩意啊?」
因此,遺傳密碼是以三個「字母」所寫成(這個三聯體被稱為密碼子[codon]),而DNA到蛋白質的連結則是以RNA作為中介物質。但是,我們仍然必須破解密碼。例如,序列為ATA TAT或GGT CAT的DNA片段,指定的是哪一對氨基酸?關於這個問題的第一條線索,出現在1961年尼倫伯格(Marshall Nirenberg)于莫斯科國際生化會議上所發表的演說。
1961年夏天的那場國際大會,聚集了分子生物界所有的重要人物,在當時默默無聞的年輕科學家尼倫伯格僅受邀演講10分鐘,而且幾乎沒有人到場聆聽,包括我在內。但是當他的驚人發現傳開后,克里克立即安插他在稍後的會議中,對著如今引頸以待的滿座觀眾發表研究結果。那一刻真是非比尋常:一個無名小卒,安靜謙遜的年輕人,在眾多分子生物學泰斗面前,指出尋找完整基因密碼之路。
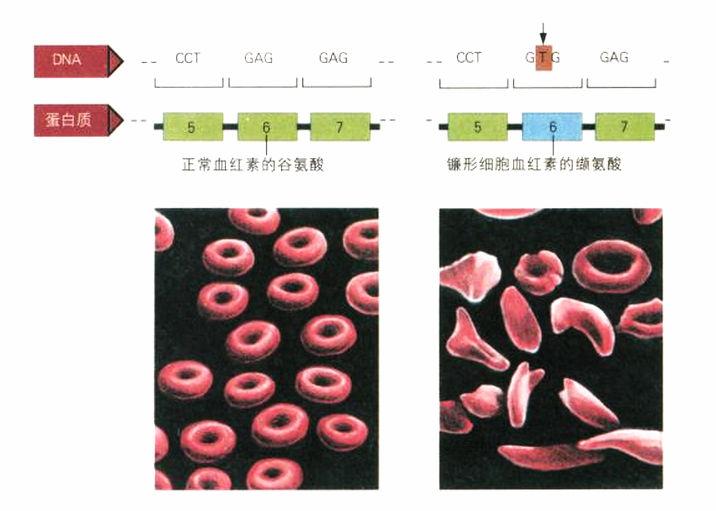
突變的重擊:人類β血紅素基因上的DNA序列里有一個鹼基發生變化,造成進入蛋白質鏈的是纈氨酸,而非谷氨酸。這個差異造成鐮形細胞貧血症,紅血球扭曲成獨特的鐮刀狀。
RNA是珍貴的進化遺產。自然選擇在解決了一個問題后,通常會繼續沿用這個解決方案,自然選擇的座右銘可以說是「沒壞就別修」。換言之,在沒有必須改變的自然選擇壓力時,細胞系統不會創新,所以會保留許多過去進化的痕迹。一個過程之所以釆取某種特定的方式,可能只因為它最初是那樣進化的,而不是因為那是最好和效率最高的方式。

左起為翟拉納、克里克及格倫伯格-馬納戈。尼倫伯格以格倫伯格-馬納戈的創新研究為基礎,在有了初步的突破后,霍拉納接續尼倫伯格,又解開許多遺傳密碼,後來兩人共同獲得諾貝爾獎。
比德爾與塔特姆發覺,果蠅對他們的研究來說太過複雜,要在像果蠅這麼複雜的生物身上找出單一突變所造成的影響,簡直是海底撈針。因此他們決定研究在各方面都簡單得多的紅麵包霉(Neurospora crassa,一種從熱帶國家的麵包上長出的橘紅色黴菌)。他們的計劃很簡單:釆取先前穆勒研究果蠅的做法,用X光照射紅麵包霉,造成突變,然後找出突變對黴菌的影響。他們追蹤突變影響的方法如下。當時已經知道,正常(未突變)的紅麵包霉可以在含有最簡單養分的基本培養基里存活,靠著這種基本食物,它們可以利用培養基里的簡單分子,以生化方式合成生存所需的較大分子。比德爾與塔特姆推論,能破壞任意一種合成路徑的突變,都會使經過X光照射的黴菌無法在基本培養基里生長;但是,如果提供它們「完整的」培養基,也就是其中包含了生存所需的所有分子,例如氨基酸與維生素,則它們應該能繼續生長。換句話說,即使突變造成黴菌無法合成某種重要的養分,但是只要能從培養基中直接取得這種養分,突變就變得無害了。
由於當時認為所有的酶都是蛋白質,因此大家很快就開始問,基因是否也為不是酶的細胞蛋白質編碼。率先提出基因可能把信息提供給所有蛋白質的,是泡令位於加州理工學院的實驗室。他和學生板野(Harvey Itano)研究血紅素(hemoglobin),這種紅血球中的蛋白質負責將氧氣從肺輸送至新陳代謝活躍的需氧組織,例如肌肉。他們專攻鐮形細胞症患者的血紅素,這種病也稱為鐮形細胞貧血症(sickle-cell anemia),是非洲人常見的基因病變,因此在非洲裔美國人中也很常見。鐮形細胞貧血症患者的紅血球細胞往往變形,在顯微鏡下呈現獨特的鐮刀狀,它們會造成微血管堵塞,使病人極為痛苦,甚至會致命。後來的研究為這種疾病常見於非洲人身上找到合理的進化解釋:由於瘧疾寄生蟲的生命周期中有一部分是在紅血球內度過,因此有鐮形細胞血紅素的人,在罹患瘧疾時,癥狀較不嚴重。人類的進化似乎替一些熱帶地區居民簽下了類似浮士德的魔鬼交易:以承受鐮形細胞造成的痛苦,換取減輕瘧疾之苦。
1956年,英格拉姆(Vernon Ingram)在鐮形細胞血紅素的研究上有進一步的發現,他的研究地點就是我和克里克發現雙螺旋的卡文迪什實驗室。英格拉姆使用新近發展出來的、可以識別蛋白質組合鏈中特定氨基酸的方法,精確找出板野和泡令所謂對分子總電荷造成影響的分子差異。這個差異起因於一個氨基酸:英格拉姆發現,在正常蛋白質鏈上第六個位置的谷氨酸,在鐮形細胞血紅素中被纈氨酸所取代。這確切證明了基因突變(在基因的DNA密碼A,T,G,C序列上的差異)可以直接「對應」到蛋白質上氨基酸序列的差異。蛋白質是生命的活躍分子,它們形成催化生化反應的酶,提供人體主要的構成要素,例如組成皮膚、頭髮與指甲的角質。DNA之所以能控制細胞、控制發育,乃至於整個生命,就是通過蛋白質。但是DNA內的編碼信息(由A,T,G,C構成的分子鏈),如何轉換至蛋白質(即氨基酸鏈)上?
儘管起頭不順,但雅各布與莫諾的合作仍締造出最傑出的科學成就。他們幹勁十足地研究大腸桿菌(E. Coli,一種常見的腸內細菌)的基因開關問題,主攻它利用乳糖(lactose)的能力。為了消化乳糖,大腸桿菌必須製造出β-半乳糖苷酶(bete-galactosidase),這種酶會將養分分解為兩種次單位,也就是更簡單的半乳糖與葡萄糖。當細菌培養基中沒有乳糖時,細胞不會製造β-半乳糖苷酶,不過加入乳糖后,細胞就會開始製造這種酶。雅各布與莫諾認為乳糖的存在會誘導β-半乳糖苷酶的產生,於是著手研究這種誘導的發生過程。
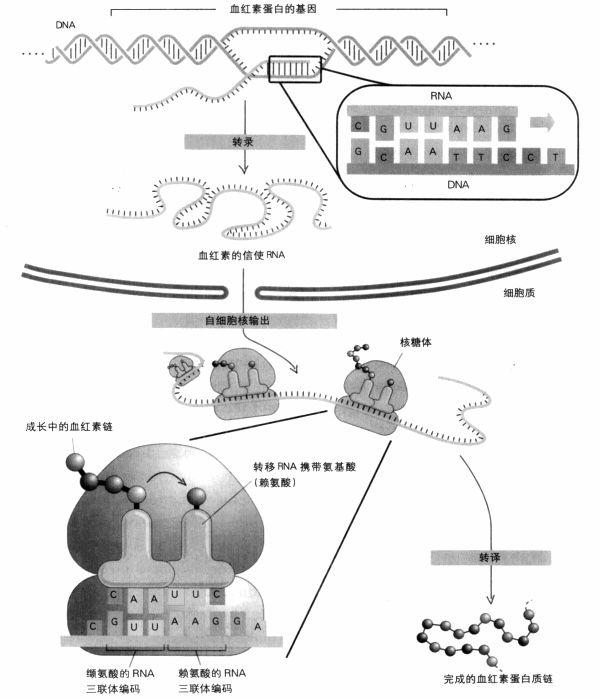
從DNA到蛋白質:DNA在細胞核內轉錄成信使RNA,然後RNA輸出至細胞質里,轉譯為蛋白質。轉譯發生在核糖體內,與信使RNA各個鹼基對三聯體密碼子互補的轉移RNA,把氨基酸帶到核糖體,這些氨基酸會結合成蛋白質鏈。
一直到1941年,比德爾(George Beadle)與塔特姆(Ed Tatum)發表了一項熱帶麵包霉的誘發突變研究時,重要進展才出現。比德爾在內布拉斯加州瓦胡(Wahoo)市郊長大,若不是高中科學老師鼓勵他朝其他領域發展,他很可能接掌家族農場。1930年代,比德爾先和以果蠅研究聞名的摩根在加州理工學院共事,再轉到巴黎生物理化研究院(Institut de Biologie Physico-Chimique),努力尋找基因如何發揮影響力,例如如何影響果蠅眼睛的顏色。他1937年來到斯坦福大學后,立即邀請塔特姆加入研究團隊,而塔特姆不顧指導教授的忠告答應了他。塔特姆在威斯康辛大學完成大學與研究所的學業,以牛奶里的細菌為研究主題(在這個乳酪之州,這個研究對象倒是不虞匱乏)儘管與比德爾共事可能會在智慧上有挑戰性,但塔特姆在威斯康辛的教授卻希望他能到乳酪農業領域就業,在經濟上比較有保障。對科學界而言,幸好塔特姆捨棄了奶油而選擇了比德爾。
在發現轉移RNA之前,一般認為所有的細胞RNA都具有模板的角色。現在我們發覺到,其實RNA有好幾種不同的形式,只不過其中最重要的是組成核糖體的兩條RNA主鏈。當時令人不解的是,根據觀察,這兩條RNA鏈的長度是固定的。如果這些鏈的確是合成蛋白質的真實模板,長度應該會隨著要合成的蛋白質的不同尺寸而異。同樣令人困惑的是,這些鏈的新陳代謝非常穩定,一旦合成后就不會崩解。然而巴黎巴斯德研究院(Institut Pasteur)的實驗卻指出,許多細菌的蛋白質合成模板都非常短命。更奇怪的是,這兩個核糖體RNA鏈的鹼基序列,似乎跟個別染色體DNA分子的鹼基序列沒有關聯https://read.99csw.com。
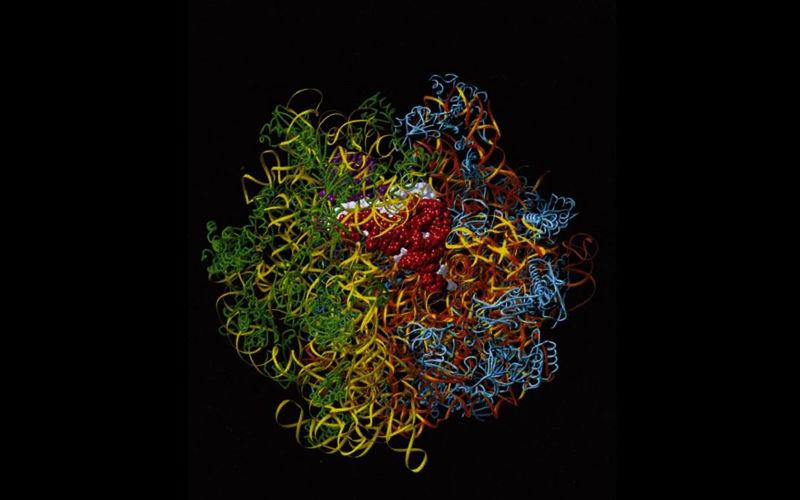
在X光分析下,細胞的蛋白質工廠核糖體呈現出壯觀的立體結構。(為了簡化之便,這個由計算機產生的影像沒有顯示原子。)每個細胞里都有數百萬個核糖體,DNA的編碼信息就是在這裏協助製造蛋白質,而蛋白質是生命分子劇本里的主角。核糖體包含由RNA構成的兩個次單位(橘和黃),另有大約60個蛋白質(藍與綠)覆在外面。圖中的核糖體正在製造蛋白質。特化的小RNA分子(紫、白與紅)將氨基酸運輸至核糖體,以加入不斷成長的蛋白質鏈。
加羅德的黑尿症也進入分子時代。1995年,研究真菌的西班牙科學家發現一種突變基因,其突變會導致加羅德在黑尿病患者的尿液中找到的物質發生累積。這個基因平常會製造一種酶,而這種酶是許多生命系統的基本配備,人類也有這種基因。比較人類與真菌的基因序列就有可能找出人類身上的這個基因,它所編碼的酶稱為尿黑酸加氧酶(homogentisate dioxy-genase)。下一步是比較正常人與黑尿病患者的基因,結果發現黑尿症患者的基因所以不起作用,是因為有一個鹼基對發生突變。加羅德所說的「先天的新陳代謝錯誤」被證明是DNA序列中的一個差異造成的。

1955年的RNA領帶俱樂部聚會,有領帶為證。左起依次為克里克、瑞奇、奧格爾(Leslie Orgel)以及沃森。
接著,信使RNA被輸送到細胞核外,來到本身就是由RNA和蛋白質構成的核糖體。在這裏,信使RNA序列中所攜帶的信息將用於製造新的蛋白質分子;這個過程即所謂的轉譯(translation)。氨基酸附著在轉移RNA上被運至現場。在轉移RNA的一端是一個特定的三聯體(71頁圖例所示為CAA),它可以找出信使RNA上跟它相對應的三聯體GUU。轉移RNA另一端拖引著跟它結合的氨基酸,在此例為纈氨酸。由於接下來的DNA序列是TTC(賴氨酸的密碼子),因此信使RNA的下一個三聯體會對應到賴氨酸的轉移RNA上。現在剩下來要做的就是以生化方法將兩種氨基酸結合在一起。重複這個過程100次,就可以製造出有100個氨基酸長度的蛋白質鏈。這些氨基酸的順序,是根據DNA上A,T,G,C的順序決定的,而信使RNA正是由此DNA所產生。兩種血紅素鏈的長度分別為141與146個氨基酸。
這個發現來自波士頓的馬薩諸塞州總醫院,在那裡任職的查美尼克(Paul Zamecnik)花了數年時間發展研究蛋白質合成的「無細胞」(cell-free)系統。細胞是高度區隔化的物體,查美尼克正確地看出,若想研究細胞內部的現象,就有必要排除細胞內多種薄膜所形成的複雜情況。他和同事使用取自老鼠肝臟組織的物質,在試管里重建簡化后的細胞環境(即「無細胞系統」),利用放射線標記追蹤合成蛋白質的氨基酸。查美尼克以這種方法找出核糖體是蛋白質的合成地點,但起初伽莫夫並不接受這個結果。
1961年,布雷納與克里克在劍橋大學以決定性的實驗證明,DNA密碼是以三聯體為基礎。他們巧妙地使用化學誘變劑來刪除或插入DNA鹼基對,結果發現插入或刪除單一一個鹼基對都會造成破壞性的「移碼」(frameshift)現象,因為在突變位置之外的所有編碼都會因此而亂掉。現在假設有一個二個字母的密碼JIM ATE THE FAT CAT(吉姆吃掉肥貓),把第一個T刪掉后,如果還要保持三個字母的密碼結構,則原句會變成JIM AET HEF ATC AT,被刪除字母以後的部分全都變成胡言亂語。如果插入或刪除兩個字母,也會造成相同的情況:刪除第一個T與E,得到的是JIM ATH EFA TCA T,這更混亂。如果刪除(或插入)三個字母呢?移除第一個A,T與E,我們得到的是JIM THE FAT CAT,雖然失去一個「單字」ATE,但是至少保留了句子里其他的字義。即使刪除的部分是分散在一個以上的單字中,例如刪除第一個T與E,以及第二個T,我們仍然只是喪失兩個單字,在它們前後的部分仍能保留:JIM AHE FAT CAT。DNA序列也是一樣:插入或刪除單一字母(一個鹼基)會對蛋白質造成很大的破壞,因為移碼效應會使插入或刪除點以外的每一個氨基酸都發生改變,而插入或刪除兩個字母的情況也一樣。但若沿著DNA分子插入或刪除三個字母,不見得會造成災難性的影響,這麼做會加入或消除一個氨基酸,但不見得會阻斷所有的生化活動。
當需要製造血紅素時,骨髓DNA的相關片段,即血紅素基因,會像DNA複製時一樣拉開雙股,但不是兩股都複製,而是只複製一股,以專業術語來說,就是轉錄(transcribe);而且在RNA聚合肽的協助下所製造的產品,不是全新的DNA股,而是新的單股信使RNA,對應血紅素基因。這時,原先產生RNA的DNA,其兩股會再度密合。
伽莫夫並不是惟一一位在理論上栽跟頭的科學家,我也有過挫敗的時候。發現雙螺旋后不久,我前往加州理工學院,想找出RNA的結構。但是負責精氨酸(arginine, ARG)的瑞奇(Alexander Rich)和我很快就發現,RNA的X光衍射圖所產生的圖案無法解釋——這個分子的結構顯然不像DNA那麼規則。同樣令人沮喪的是,在一封1955年初發給所有領帶俱樂部會員的記錄中,負責酪氨酸(tyrosine, TYR)的克里克預測,DNA→蛋白質的轉型秘密並不是隱藏在RNA的結構中,這跟我想的不同。他認為氨基酸可能是由所謂的轉接分子(adaptor molecule)帶往合成蛋白質的實際位置的,而且每一種氨基酸都有特定的轉接分子。他推測這些轉接物本身可能是非常小的RNA分子。我拒絕接受他的推理達兩年之久,後來一個極度意外的生化發現,證實了他的創新觀點正中目標。
然而,大多數DNA領域的先驅仍選擇繼續去研究基因功能的基本機制。為什麼有些蛋白質特別多?許多基因只在特定的細胞或細胞生命的特定時間才會啟動,這是怎麼辦到的?以肌細胞與肝細胞為例,二者無論是功能或是顯微鏡下的外觀,都大不相同。基因在表現(發揮功能)上的變化,造成了細胞的多樣性與分化。肌細胞與肝細胞最根本的差異是,它們製造不同的蛋白質,而要製造不同的蛋白質,最簡單的方法是控制每個細胞里要轉錄哪些基因。因此,所有的細胞中都有所謂的「家務蛋白質」(housekeeping protein),它們對於細胞的運作相當重要,例如參与DNA的複製。此外,特定細胞內的某些基因會在特定時刻啟動,以製造適當的蛋白質。我們也可以把「發育」這種從一個受精卵變為極度複雜的成熟個體的生長過程,視為一長串浩大的基因開關作用。隨著在發育過程中產生各種細胞組織,一組基因必然會不斷被開啟和關閉。
雅各布與莫諾藉由研究大腸桿菌的變種而九*九*藏*書得到這些結果。他們並未找到抑制子存在的直接證據,只是從基因調控之謎的解答中,根據邏輯推斷出它的存在。一直到20世紀60年代晚期,哈佛大學的吉爾伯特(Walter Gilbert)與穆勒-希爾(Bernio Mǖller-Hill)實際分離出抑制子並進行分析,雅各布與莫諾的想法才在分子領域得到證實。他們僅預測它的存在,但吉爾伯特與穆勒-希爾卻真的找到它。抑制子的數量通常極少,每個細胞只有少量而已,因此想收集到足夠分析使用的數量就是一項技術挑戰,但他們終究辦到了。與此同時,在同層樓另一間實驗室工作的普塔什尼(Mark Ptashne)也成功分離出另一個抑制子,並且找出其特性,這次是在噬菌體的基因開關係統找到的。原來抑制子是能與DNA結合的蛋白質。在大腸桿菌的例子中,缺乏乳糖時,β-半乳糖苷酶的抑制子會結合至大腸桿菌DNA上,也就是β-半乳糖苷酶基因的轉錄起始位置附近,讓根據這個基因來製造信使RNA的酶無法發揮作用。不過在加入乳糖后,乳糖會與抑制子結合,使它無法佔據DNA分子上靠近半乳糖苷酶基因的位置,如此一來,轉錄就可以自由進行了。
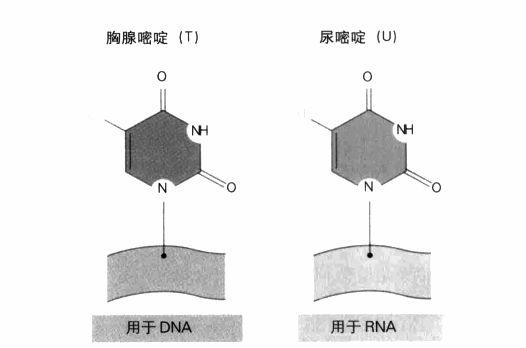
遺傳密碼,顯示了決定信使RNA序列的三聯體序列。DNA與RNA之間有一個重要差異,即DNA使用胸腺嘧啶(T),RNA則使用尿嘧啶(U),如左圖所示。這兩個鹼基都與腺嘌呤(A)互補。終止密碼子的作用正如其名:它們表示基因編碼的結束。
有一天深夜,克里克和同事巴奈特(Leslie Barnett)一起到實驗室查看三聯體刪除實驗的最終結果,他立刻意識到這個結果的重要性,於是告訴巴奈特:「全球只有你和我知道,它是三聯體編碼!」克里克和我是最先窺見生命雙螺旋秘密的人,現在他又成為最先確認這個秘密是以三字碼撰寫的人。
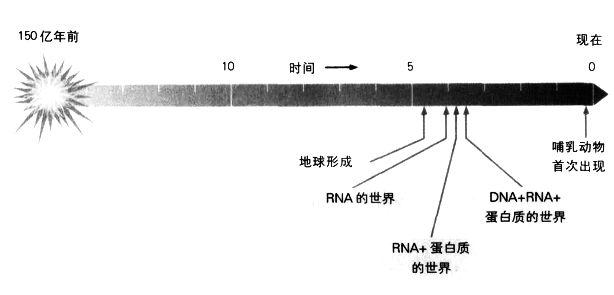
太初宇宙大爆炸后的生命進化。我們可能永遠無法確定生命起源的精確時間,但是最早的生命形態很可能完全以RNA為基礎。
要找到蛋白質製造過程的重要線索,似乎應該進一步研究RNA,而不是DNA。為了鼓勵大家「破解密碼」,也就是解開DNA序列和蛋白質上氨基酸序列的謎樣關係,我和伽莫夫創立了「RNA領帶俱樂部」(RNA Tie Club)。由於只有20種氨基酸,所以俱樂部成員人數限制在20人,各代表一個氨基酸。伽莫夫設計了俱樂部的領帶,並且委託工廠製造代表特定氨基酸的領帶夾,作為職位徽章。每個領帶夾上都有特定氨基酸的三個字母縮寫,配戴有哪種氨基酸縮寫的領帶夾,就負責研究哪種氨基酸。我拿的是脯氨酸(proline, PRO),伽莫夫的是丙氨酸(alanine, ALA)。在那個年代,領帶夾上的字母通常是姓名的縮寫,伽莫夫也樂得用他的ALA領帶夾來迷惑別人。結果他反而整到自己,有次一位眼尖的旅館收銀員就拒收他的支票,因為支票上的名字和他領帶夾上的縮寫完全無關。
板野與泡令比較鐮形細胞貧血症患者與正常人的血紅素,發現這兩種分子的差異在於電荷。當時正值1940年代晚期,遺傳學家認為鐮形細胞貧血,是以孟德爾典型的隱性性狀來遺傳的。於是他們推論,鐮形細胞貧血必然是血紅素基因發生突變所引起的,這種突變對血紅素的化學組成造成影響。因此泡令重新修正加羅德所說的「先天的新陳代謝錯誤」,認為有些是「分子疾病」。鐮形細胞貧血正是一種分子疾病。
不久,在同事霍格蘭(Mahlon Hoagland)的協助下,查美尼克甚至有了更驚人的發現,那就是氨基酸在形成多肽鏈之前,是與小RNA分子相結合的。起初他們對這結果感到迷惑,直到聽我說起克里克的轉接分子理論才恍然大悟。接著他們很快證實了克里克的想法,亦即每一種氨基酸都有特定的RNA轉接分子,稱為轉移RNA (transfer RNA,簡稱tRNA)。每一個轉移RNA分子的表面都有特定的鹼基序列,能連接至對應的RNA模板片段,從而在蛋白質合成時,依序排列氨基酸。
找出抑制子的分子特性后,讓我們對支撐生命的分子作用過程有了完整的了解。我們原先已經知道DNA通過RNA來製造蛋白質,到了這時,我們也知道蛋白質可以通過和DNA結合,直接和DNA產生交互作用,進而調控基因的活動。
當時對編碼計劃感興趣的科學家大半可以擠入這個限制在20人的俱樂部,可見那時的DNA-RNA學界真的很小。伽莫夫輕易就替非生物學家的好友、物理學家特勒(Edward Teller)找到一個位置,由他負責研究亮氨酸(leucine, LEU),我則引介費曼(Richard Feynman)來研究甘氨酸(glycine, GLY)。費曼任職于加州理工學院,是極富創意的物理學家,他在研究原子力遇到挫折時,經常到生物大樓來找我。

雅各布、莫諾與利沃夫(左起)
實際上,尼倫伯格與馬特伊只解決了1/64的問題,當時我們只知道UUU是為苯丙氨酸編碼的密碼子,還有63組三個字母的密碼子尚待解開。接下來的數年,掀起一股研究熱潮,大家都努力尋找其他密碼子代表的是哪個氨基酸。當時的棘手問題在於如何合成RNA的各種排列組合。UUU(聚尿嘧啶)算是很單純的,較易製造,但是AGG呢?許多巧妙的化學方法都是為了解決這些問題而設計出來的,其中有不少出自威斯康辛大學的霍拉納(Gobind Khorana)之手。到了1966年,64個密碼子各自指定哪一個氨基酸的秘密(即遺傳密碼本身)都已解開。1968年,霍拉納與尼倫伯格榮獲諾貝爾生理醫學獎。
比德爾與塔特姆照射了大約5000個樣本,一一試驗它們是否能在基本培養基中存活。第一個樣本存活得很好,第二個也是,然後第三個……一直試到第299個,他們才找到無法在基本培養基中存活的菌株,不過如同預期,它能夠在完整的培養基里生存。第299號菌株成為他們分析的第一個突變菌株,其後又分析了更多。下一步是找出這些突變種喪失的究竟是哪一種能力。或許第299號菌株無法生存,是因為無法合成必要的氨基酸。於是比德爾和塔特姆將氨基酸加入基本培養基,但是第299號仍舊無法生長。會不會是維生素呢?他們又將大量維生素加入基本培養基,這次第299號終於成功生長。接著他們開始縮小範圍,每次只加入一種維生素,然後量測299號的生長反應。加入煙鹼酸,沒反應,核黃素也不管用,一直到加入維生素B6時,第299號才能在基本培養基中生存。X射線對第299號造成的突變,不知何故中斷了製造B6的合成路徑。但這究竟是如何造成的?比德爾與塔特姆知道,這類生化合成過程是由蛋白質酶所控制的,它們會催化合成路九九藏書徑中個別的化學反應,因此他們認為自己發現的每個突變都會破壞特定的酶。而既然突變發生在基因上,酶肯定是基因製造的。當他們在1941年發表研究結果時,形成了一句流行標語,而它也總結出對基因運作的理解:「一種基因,一種酶。」
等到1954年我和伽莫夫首次見面時,他已想出一套理論。根據他的說法,DNA鹼基的重疊三聯體可以「指定」特定的氨基酸。他的理論基礎在於他認為每個鹼基對的表面都有一個空洞,而這個空洞的形狀剛好跟氨基酸表面一部分的形狀互補。我告訴伽莫夫,我對這一點感到懷疑,氨基酸在連結成鏈(稱為多肽鏈)之前,不可能直接以DNA為其排序的模板。伽莫夫是物理學家,我想他可能沒看過相關論文——一些科學論文曾指出,蛋白質合成作用不可能發生於DNA所在位置(即細胞核)。事實上,科學家曾觀察到,移走細胞內的細胞核,並不會立即影響蛋白質的製造速度。今日我們已經知道氨基酸是在核糖體(ribosome)內組合成蛋白質,核糖體是包含RNA這第二種形式的核酸的細胞內小粒子。

RNA領帶俱樂部的第一封公函:信上列出20位會員隨機分配到的氨基酸領帶夾。這封信是伽莫夫發給沃森的,信末有伽莫夫親筆字跡。信頭底下印著俱樂部的箴言:「不成功便成仁,不然乾脆啥也別做。」
雅各布也參戰了,他逃往英國,加入戴高樂將軍的自由法國軍。他在北非服役,參与了諾曼底登陸。登陸不久,他就差點被炸死,從他身上一共取出20塊炸彈碎片,但至今仍有80個彈片留在他身上。由於手臂受傷,他無法實現當外科醫生的抱負,後來他跟我們這一代許多人一樣,在薛定諤的《生命是什麼?》影響下,轉而研究生物學。不過,他想加入莫諾的研究團隊,卻屢次遭到拒絕。按照雅各布本人的說法,在嘗試七八次后,1950年6月,莫諾的老闆、微生物學家利沃夫(André Lwoff)終於同意讓他加入:
在了解基因如何開啟和關閉上,第一個重要進展來自20世紀60年代巴黎巴斯德研究院的雅各布與莫諾(Jacques Monod)所做的實驗。莫諾在科學界起步較慢,這可憐的傢伙因為在許多領域都很有天賦,反而無法專心致志。20世紀30年代時,他在加州理工學院的生物系師從果蠅遺傳之父摩根,但是儘管天天與摩根那群早已不再年少的「孩子們」相處,也沒能讓他皈依果蠅研究。他反倒比較喜歡在大學和當地百萬富翁的豪宅里指揮巴哈演奏會,後來校方還聘請他教授大學部的音樂欣賞課程。一直到1940年,他才在巴黎索邦大學(Sorbonne)完成博士學業,不過這時他已積極投入法國地下組織的反抗運動。莫諾曾把重要的秘密文件藏在實驗室外長頸鹿標本中空的腿骨內,這是歷史上罕見的利用生物學來從事的間諜活動。隨著戰爭進展,他對反抗組織的重要性也與日俱增(也更容易遭納粹搜捕)。到了諾曼底登陸時,他在協助盟軍進攻與逼迫德軍撤退上作出很大貢獻。
不過當時遺傳密碼仍隱晦難解,我們不明白核酸的序列是根據什麼規則轉譯為規律的多肽序列的。在RNA領帶俱樂部1956年一份文件中,布雷納提出了一些理論問題,要點如下:在只有4個DNA字母(A、T、G、C)的情況下,這套密碼要如何指定由20個氨基酸中的哪一個接在某一點上來組成蛋白質鏈?一個核苷酸,因為只有4種變換身份的可能性,顯然是不夠的。即使兩個核苷酸,也只有16(4×4)種可能,仍然不夠用。因此,至少要三個核苷酸一組,形成三聯體,才可能為每個氨基酸編碼。但是這會造成令人不解的重複對應問題。以三聯體來編碼,有64種排列的方式(4×4×4),但是氨基酸只有20個,這是否代表大多數的氨基酸可以由一個以上的三聯體來編碼?若是如此,用「四聯體」來編碼,總共可以有256種(4×4×4×4)排列方式,原則上應該也適用,只不過這樣的話,重複對應的情況會更多。
我和克里克發表關於雙螺旋的說明后不久,陸續收到俄羅斯出身的知名理論物理學家伽莫夫(George Gamow)的來信。他總是親筆寫信,還會加一些漫畫和塗鴉,有些與內容有關,有些沒多大關係。他在信上的署名總是一個簡單的「Geo」(後來我們才發現它的發音是jo)。他對DNA產生興趣,而且早在英格拉姆確切證明了DNA的鹼基序列和蛋白質的氨基酸序列之間的關聯時,就開始對DNA和蛋白質的關係感到好奇。伽莫夫體會到生物學終將成為一門精密科學,並且預言未來所有生物的遺傳密碼都能用一長串以1,2,3,4構成的數字來表示,這4個數字各自代表一個鹼基(A,T,G,C)。起初我們以為他在說笑,完全忽視他的第一封信。不過幾個月後,當克里克在紐約市碰到他時,清楚地看出他驚人的才能,而我們也立即歡迎他登上DNA的列車,成為最早上車的乘客之一。
利沃夫沒再給我機會多談談我的希望、無知與熱誠,他宣布說:「我們發現了原噬菌體的誘導現象!」(「原噬菌體的誘導現象」指如何啟動已經整合入宿主細菌DNA中的噬菌體DNA。)
然後他問:「你對研究噬菌體有興趣嗎?」我結結巴巴地說這正是我想作的研究。「很好,那你就9月1日過來吧。」
| 遺傳密碼 | |
|---|---|
| 氨基酸 | RNA密碼子 |
| 丙氨酸 | GCA GCC GCG GCU |
| 精氨酸 | AGA AGG CGA CGC CGG CGU |
| 天冬酰氨 | AAC AAU |
| 天冬氨酸 | GAC GAU |
| 半胱氨酸 | UGC UGU |
| 谷氨酸 | GAA CAG |
| 谷酰胺酸 | CAA CAG |
| 甘氨酸 | CAA CAG |
| 組氨酸 | CAC CAU |
| 異亮氨酸 | AUA AUC AUU |
| …… | …… |
這些發現無意間解決了生命起源中「先有雞,還是先有蛋」的問題。許多人認為,最早的生命形式是由一個DNA分子所構成的,這個盛行的假設有一個無法避免的矛盾之處:DNA無法自行聚合,它需要蛋白質才能聚合。那麼究竟是先有蛋白質,還是先有DNA?若是先有蛋白質,據我們所知,蛋白質卻不具備複製信息的方法;若是先有DNA,DNA是可以複製信息,但必須要有蛋白質才行。這是個無解的問題。當時我們認為,要有DNA,就必須有蛋白質;而要有蛋白質,就必須有DNA。